工业制硝酸是一项重要的化学工艺,硝酸作为一种广泛应用的化学品,在农业、医药、化工、炸药等多个领域都有着重要的应用。本文将介绍工业制硝酸的过程及应用。
一、硝酸的物理性质和化学性质
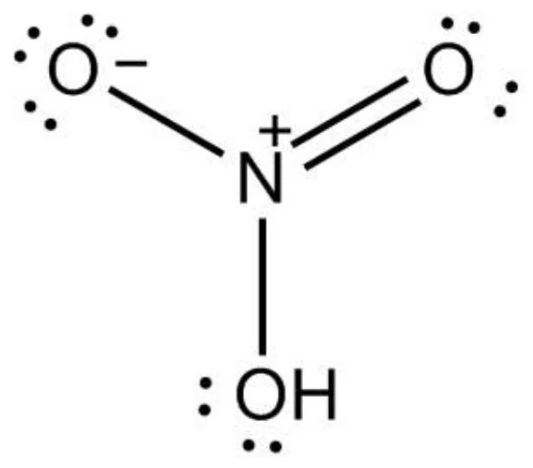
硝酸又称为硝基酸,化学式为HNO3,是一种无色、透明、具有刺激性气味的液体,密度为1.51g/cm3,沸点83℃。硝酸是一种强酸,能够与金属、非金属及有机物发生反应,产生丰富的化学性质。硝酸的主要化学性质包括:
1.氧化性:硝酸是一种强氧化剂,在与其他物质反应时常常起氧化作用。
2.还原性:在适当条件下,硝酸也可以被还原成氮气。
3.亲电性:硝酸的分子中带有极性的氧元素和氮元素,因此具有较强的亲电性。
4.腐蚀性:由于硝酸是一种强酸,能够与许多物质发生反应,因此具有较强的腐蚀性。
二、硝酸的制备
1. 硝酸的制备方法
硝酸的制备方法有两种:硝酸铵法和氧化氮法。
硝酸铵法是最早被应用的制备硝酸的方法,其主要原理是硝酸铵在加热时分解放出氨气和一定量的氧气,氧气和水反应生成硝酸。硝酸铵法的反应方程式如下:
NH4NO3 → N2O + 2H2O N2O + O2 + H2O → 2HNO3
氧化氮法是现代工业中普遍采用的制备硝酸的方法,其主要原理是以氧化氮为原料,在一定条件下催化反应生成硝酸。氧化氮法的反应方程式如下:
NO + 1/2O2 + H2O → HNO3
2. 硝酸的制备流程
硝酸的制备流程主要包括以下几个步骤:
(1)硝酸铵法
硝酸铵法的制备流程如下:
a. 将氨气和硝酸加入反应釜中并混合均匀,然后加热至70℃左右。
b. 在加热过程中,硝酸铵分解放出氨气和一定量的氧气。
c. 氧气和水反应生成硝酸。
(2)氧化氮法
氧化氮法的制备流程如下:
a. 将氮气和氧气混合后通过催化剂床。
b. 在催化剂的作用下,氮气和氧气发生反应生成氧化氮。
c. 氧化氮通过冷却、吸收、浓缩等处理步骤生成硝酸。
三、硝酸的应用
硝酸作为一种广泛应用的化学品,在多个领域都有着重要的应用。
1. 农业
硝酸在农业领域中主要用于合成化肥,如硝酸铵、硝酸钾等。这些化肥能够为植物提供氮元素,促进植物生长。
2. 医药
硝酸在医药领域中主要用于制备药物,如硝酸甘油、硝酸银等。这些药物能够用于治疗心脏病、感染等疾病。
3. 化工
硝酸在化工领域中主要用于制备其他化学品,如硝基苯、硝酸纤维素等。这些化学品广泛应用于染料、涂料、塑料等行业。
4. 炸药
由于硝酸具有强氧化性,因此在炸药制备中也有广泛应用。硝酸能够与其他物质反应生成炸药,如硝化甘油、TNT等。
工业制硝酸是一项重要的化学工艺,硝酸作为一种广泛应用的化学品,在农业、医药、化工、炸药等多个领域都有着重要的应用。硝酸的制备方法主要有硝酸铵法和氧化氮法,硝酸的制备流程包括加热、分解、反应等步骤。在应用方面,硝酸广泛应用于农业、医药、化工、炸药等多个领域,对社会经济发展有着重要的推动作用。




















 浙公网安备
33020502000290号
浙公网安备
33020502000290号

